Что такое болезнь Альцгеймера?
Болезнь Альцгеймера (БА) — это заболевание, которое вызывает гибель клеток головного мозга. Со временем когнитивные способности человека начинают заметно ухудшаться: появляются провалы в памяти, проблемы с речью и трудности с ориентированием в пространстве.
БА является самой распространенной причиной деменции. Согласно данным ВОЗ, в 2021 году насчитывалось более 55 млн людей, живущих с этой болезнью. Ожидается, что к 2030 году количество больных достигнет 78 млн, а к 2050 — до 139. Несмотря на широкое распространение, точные причины заболевания до сих пор остаются неясными. Болезнь Альцгеймера — это яркий пример нейродегенеративного заболевания, при котором состояние пациента постепенно только ухудшается.
Современная медицина все еще не может остановить развитие болезни, но способна замедлить ее прогресс. Поэтому ранняя диагностика заболевания крайне важна: она помогает избежать неподходящих методов лечения и подобрать правильный план оказания помощи. В отличие от БА, некоторые типы деменции поддаются лечению. Например, деменция при гипотиреозе успешно лечится благодаря нормализации уровня гормонов щитовидной железы.
Диагностика болезни сейчас
Методы выявления болезни Альцгеймера можно разделить на две группы: дорогостоящие и сложные, но дающие точный результат, и более доступные и простые, но менее достоверные.
В первую категорию входят методы нейровизуализации — позитронно-эмиссионная томография (ПЭТ) и магнитно-резонансная томография (МРТ). Они позволяют получить детализированные изображения мозга, на которых можно заметить изменения, характерные для БА. Так, ПЭТ-сканирование позволяет оценить, как работают некоторые нейроны, а также определить уровень нейротоксинов в отдельных участках мозга. МРТ же помогает исключить другие мозговые нарушения и оценить степень атрофии мозга. Еще один точный способ диагностики — измерение уровня тау-белка и β-амилоида в спинномозговой жидкости. Однако этот метод требует болезненной процедуры, сопряженной с рисками для здоровья.
Существуют и более доступные методы диагностики, такие как опросники для оценки когнитивных функций (Mini Mental State Examination или Краткую шкалу оценки психического статуса, MoCA-тест) и нейропсихологические тесты (например, тест «4 горы», который оценивает пространственную память). Эти способы более просты в использовании и менее затратны. Однако их точность невысока, так как результаты могут зависеть от субъективной интерпретации специалиста. Также к числу относительно доступных методов можно отнести генотипирование, которое позволяет выявить наличие вариантов, связанных с риском развития болезни Альцгеймера, и анализ крови на биомаркеры, который может дать информацию о вероятности заболевания. Но без дополнительных исследований их результаты тоже не являются надежными. Для скрининга, который необходим для выявления заболевания на ранней стадии, ни один из перечисленных методов не подходит.
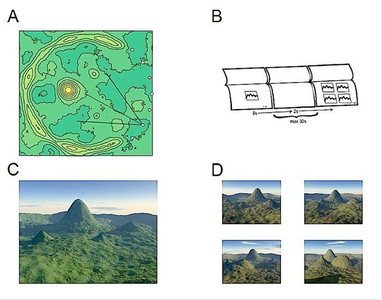
Изображение теста «4 горы», который оценивает пространственную память
Раннее распознавание
Ранняя диагностика заболевания имеет огромное значение. Она дает возможность начать лечение болезни тогда, когда еще есть шанс замедлить ее развитие. Это, в свою очередь, дает пациентам и их близким время подготовиться к предстоящим изменениям, связанным с БА. К тому же, если своевременно обнаружить проблему, можно значительно сократить расходы на ее лечение. Так как запоздалая диагностика часто влечет за собой более тяжелые осложнения, их лечение требует больших финансовых трат. Но на ранних стадиях заболевание часто остается незамеченным, поскольку его симптомы принимают за естественные признаки старения. Однако своевременная диагностика возможна. Так, в 2021 году в Швеции было проведено исследование, которое показало, что при комбинировании анализа крови и трех когнитивных тестов можно выявить маркеры болезни, предсказывающие ее развитие даже на ранних стадиях. Тем не менее такой сложный анализ невозможно использовать для масштабного скрининга.
Речевые нарушения как предвестник деменции
Исследования последних лет показали, что на ранних стадиях болезни Альцгеймера могут наблюдаться небольшие речевые нарушения, которые возникают за много лет до того, как становятся заметны другие когнитивные ухудшения.
БА отличается от других видов деменции особенностями речи, которые служат важным индикатором заболевания. Одной из ключевых речевых особенностей является аномия — затруднение в подборе слов. Человек может испытывать трудности с поиском нужного слова и заменять его обобщающими понятиями. Например, «транспорт» вместо «автобус» или «фрукт» вместо «яблоко». При этом больной способен различать слова, связанные по смыслу. В отличие от этого, семантическая деменция характеризуется воспроизведением слов, понимание которых нарушено.
Также у пациентов, страдающих БА, могут возникать трудности с пониманием предложений, появляться больше пауз в речи и наблюдаться проблемы с построением информативных связных повествований. Во время рассказа человек может делать частые скачки с одной темы на другую и чаще использовать местоимения, чем существительные. Для нормального старения такие особенности нехарактерны. Пожилые люди могут забывать наименования предметов и говорить, делая паузы, более медленно, однако в их речевом поведении чаще отмечают самоисправления и повторы, фрагментацию высказываний и использование простых предложений.
Врачи, использующие традиционные методы обнаружения заболевания, не могут уловить едва заметные речевые изменения. Для этого нужны новые технологии, которые позволят более точно диагностировать болезнь.
ИИ в помощь
Использование методов обработки естественного языка (NLP) и распознавания речи обещает сделать диагностику менее инвазивной и затратной. К тому же это позволит быстрее выявлять болезнь на ранних стадиях.
Исследования показывают, что с помощью моделей машинного обучения возможно выявить корреляцию между изменениями в речи и прогрессированием заболевания. Из записей голосов пациентов длительностью всего в несколько минут можно получить ценную информацию о моторном контроле речи и грамматической сложности. Это значительно эффективнее привычных когнитивных тестов.
Также автоматическая диагностика по речи может сделать процесс более доступным. Традиционные методы требуют лабораторных исследований, в то время как для анализа речи можно просто использовать записи голоса пациента.
Какие данные используют для обучения машинные модели?
Для обучения машинных моделей применяются разнообразные наборы данных, созданные специально для выявления когнитивных нарушений, связанных с БА. Их можно классифицировать по типу речевых данных, на которых они базируются.
Первая категория включает спонтанную речь. Наиболее известным заданием из этой категории является описание картинки с кражей печенья. Это задание позволяет оценить семантические знания и навыки повествования участников, давая им возможность описать сложную картинку. Такие датасеты, как Pitt Corpus, Delaware Corpus, ADReSS и ADReSSo, содержат задания этого типа. Архив транскрибированных аудио- и видеоматериалов The Carolina Conversations Collection содержит другую форму спонтанной речи — свободную беседу. Такой подход считается максимально приближенным к реальности, что позволяет анализировать применение языка в повседневном контексте.

Картинка с кражей печенья, предназначенная для задания на спонтанную речь
Теперь перейдем ко второй категории. В нее входят задания на беглость речи, которая делится на два типа: фонематическую и семантическую. Задания на фонематическую беглость проверяют умение пациентов за ограниченный промежуток времени составлять слова, начинающиеся с одной буквы, а задания на семантическую — умение произносить слова из заданной категории. Подобные задания есть среди аудиоданных Framingham Heart Study.
И, наконец, третья категория включает письменные работы людей, страдающих деменцией. Эта информация ценна тем, что может отражать динамику языковых изменений, происходящих с течением времени. Например, Dementia Blog Corpus был составлен на основе публичных блогов пациентов с деменцией, а Multimodal Dementia Corpus включает как напечатанные, так и написанные от руки тексты пациентов.
Достижения и ограничения
Результаты применения ИИ для диагностики болезни Альцгеймера по речи поистине поражают. В настоящее время существуют разные модели машинного обучения, способные выявить едва заметные лингвистические изменения и поставить диагноз: и традиционные модели вроде SVM и логистической регрессии, и модели глубокого обучения. Они обучаются как на транскрибированных текстах, так и на аудиоданных, и способны анализировать различные признаки: частоту голоса, синтаксическую сложность, беглость речи, количество пауз, лексическое разнообразие и фонетические паттерны. Точность (accuracy) распознавания БА по речи с помощью различных нейронных сетей составляет не менее 70,7%. А наивысшую точность классификации — 97,18% — продемонстрировала нейросеть-трансформер BERT, дообученная на автоматически расшифрованных записях речи.
Чтобы определить, насколько хорош этот показатель, давайте сопоставим его с результатами другого простого метода, который можно применять на ранних стадиях заболевания, — анализа крови. Недавние исследования продемонстрировали, что метод обнаружения биомаркеров в плазме крови имеет точность около 90%. Это впечатляющий результат, но нейронные сети все-таки его превосходят.
И все же автоматическая диагностика неидеальна. Во-первых, большая часть датасетов составлена на английском, что существенно снижает вероятность помощи людям, не говорящих на этом языке. Во-вторых, на данный момент датасеты имеют небольшие размеры. Это может снизить точность и затруднить интерпретацию, ведь с ограниченным количеством информации становится тяжело выявить все возможные значимые закономерности. Данные маленького размера не отражают разнообразие речевых проявлений болезни.
А что, если бы мы могли диагностировать болезнь Альцгеймера до появления первых симптомов? Возможно, в недалеком будущем искусственный интеллект сможет определять болезнь еще до того, как произойдет необратимое повреждение мозга или снижение умственных способностей. Такая инновация открыла бы новые горизонты для медицины и в конечном итоге помогла бы миллионам людей сохранить их качество жизни.
Источники
- Вишняков В. А., Чуйэ Ю. ИТ-диагностика болезни Альцгеймера на основе анализа голосовой информации // Проблемы инфокоммуникаций. 2023. № 2 (18). С. 66–71.
- Calzà L., Gagliardi G., Favretti R., Tamburini F. Linguistic features and automatic classifiers for identifying mild cognitive impairment and dementia // Computer Speech & Language. 2021. Vol. 65. P. 101113.
- Cera M., Ortiz K., Bertolucci P., Tsujimoto T., Minett T. Speech and phonological impairment across Alzheimer’s disease severity // Journal of Communication Disorders. 2023. Vol. 105. P. 106364.
- Ding K., Chetty M., Noori Hoshyar A. et al. Speech based detection of Alzheimer’s disease: a survey of AI techniques, datasets and challenges // Artificial Intelligence Review. 2024. Vol. 57. P. 325.
- Eyigoz E., Mathur S., Santamaria M., Cecchi G., Naylor M. Linguistic markers predict onset of Alzheimer’s disease // EClinicalMedicine. 2020. Vol. 28. P. 100583.
- Palmqvist S., Tideman P., Cullen N. et al. Prediction of future Alzheimer’s disease dementia using plasma phospho-tau combined with other accessible measures // Nature Medicine. 2021. Vol. 27. Pp. 1034–1042.
- Юйсинь М. Особенности речевого поведения пожилых людей в русскоязычной коммуникации // Современное педагогическое образование. 2023. № 6. С. 226–230.
- Kempler, D., Goral, M. Language and dementia: Neuropsychological aspects // Annual review of applied linguistics. 2008. No. 28. С. 73–90.
- Коваленко Е.А., Махнович Е.В., Первунина А.В. и др. Биомаркеры крови в ранней диагностике болезни Альцгеймера // Эффективная фармакотерапия. 2023. № 19 (45). С. 30–36.
- Palmqvist S., Tideman P., Mattsson-Carlgren N., et al. Blood biomarkers to detect Alzheimer disease in primary care and secondary care // JAMA. 2024. Vol. 332 (15). Pp. 1245–1257.
- Всемирная организация здравоохранения [Электронный ресурс] // 2025. URL: https://www.who.int/ru/news/item/02-09-2021-world-failing-to-address-dementia-challenge (дата обращения: 21.12.24).
- DementiaBank English Pitt Corpus [Электронный ресурс] // URL: https://dementia.talkbank.org/access/English/Pitt.html (дата обращения: 07.02.25).
- DementiaBank English Protocol Delaware Corpus [Электронный ресурс] // URL: https://dementia.talkbank.org/access/English/Protocol/Delaware.html (дата обращения: 07.02.25).
- Saturnino L., Fasih H., Sofia de la F., Davida F., Brian M. Alzheimer’s Dementia Recognition through Spontaneous Speech: The ADReSS Challenge // INTERSPEECH. 2020.
- Saturnino L., Fasih H., Sofia de la F., Davida F., Brian M. Detecting cognitive decline using speech only: The ADReSSo Challenge [Электронный ресурс] // 2023. DOI: https://doi.org/10.48550/arXiv.2104.09356. URL: https://arxiv.org/abs/2104.09356 (дата обращения: 07.02.25).
- The Carolina Conversations Collection [Электронный ресурс] // 2009–2016. URL: https://carolinaconversations.musc.edu/ccc/about/ (дата обращения: 07.02.25).
- Framingham Heart Study [Электронный ресурс] // URL: https://www.framinghamheartstudy.org/ (дата обращения: 07.02.25).
- Dementia Blog Corpus [Электронный ресурс] // URL: https://github.com/vmasrani/blog_corpus (дата обращения: 07.02.25).
- Multimodal Dementia Corpus [Электронный ресурс] // URL: https://arxiv.org/html/2109.01537v2/#S1 (дата обращения: 07.02.25).
- Table 6 Comparisons of research on ADReSSo dataset [Электронный ресурс] // URL: https://link.springer.com/article/10.1007/s10462-024-10961-6/tables/6 (дата обращения: 25.12.24).


